传统认知正被新技术颠覆,长效存活机制浮出水面
长期以来,干细胞领域存在一个“共识”:间充质干细胞(MSC)进入人体后只是“短暂过客”,存活几天到几周就会被免疫系统清除。然而,随着活体示踪技术的进步,这一认知正在被改写。最新研究表明,在特定条件下,MSC在体内可存活长达4个月(120天)以上,甚至持续发挥治疗作用。

一、旧认知:MSC是“短命”的过客吗?
在常规理解中,MSC的体内旅程往往被认为很短暂:
静脉输注:大部分细胞会滞留于肺部,存活时间多以天计算,部分研究显示数周内被清除。
局部注射:在关节腔或组织内,存活时间可延长至数周,但长期定植仍较困难。
这种“短效”印象主要源于早期的检测技术限制,以及免疫系统对外源性细胞的快速清除机制。许多学者曾认为,MSC的作用主要依赖于短期内的“旁分泌效应”(分泌细胞因子),而非长期驻留。
二、新证据:120天并非天方夜谭
近年来的高质量研究通过更精准的示踪技术(如萤火虫荧光素酶系统、MRI纳米追踪),证实了MSC具备长期存活的潜力。
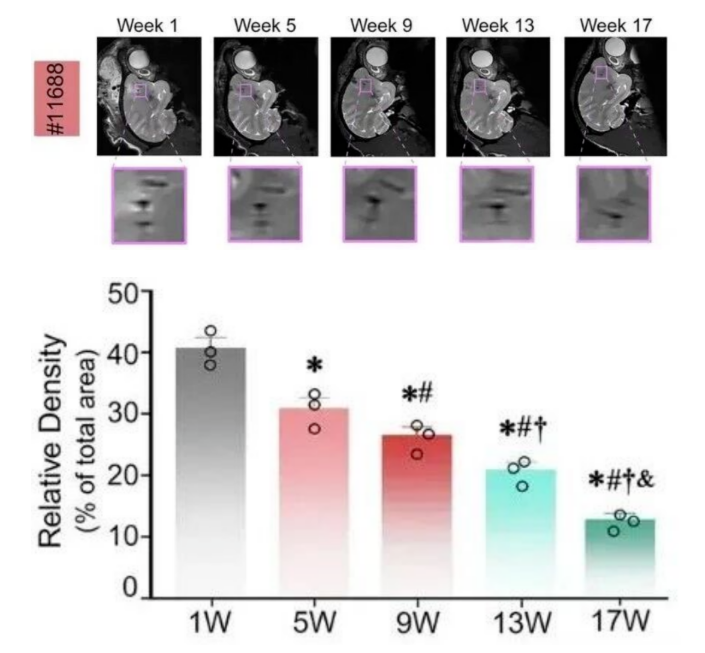
1、脑内立体定向移植:存活17周
一项针对缺血性脑卒中模型的研究显示,通过立体定向注射技术将人脐带来源MSC移植到猴脑梗塞区域,细胞存活了整整17周(约4个月)。通过MRI和病理染色确认,这些细胞不仅存活,还持续表达SDF-1(CXCL12)等修复因子,促进神经再生。这表明在免疫豁免的脑组织及精准移植下,长期存活完全可行。
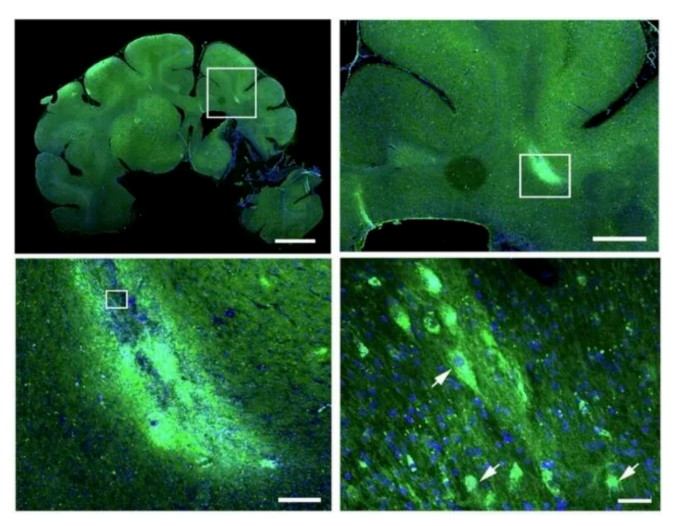
2、免疫缺陷模型:持续4个月表达酶
在针对黏多糖贮积症(MPS VII)的基因治疗研究中,慢病毒修饰的人骨髓MSC在免疫缺陷小鼠体内至少持续存在了4个月,并持续表达治疗水平的β-葡萄糖醛酸酶,显著改善了模型动物的病理状况。
3、皮下移植模型:存活超6个月
国内研究团队将EGFP标记的脐带MSC注射至裸鼠皮下,虽然荧光强度在7天后下降,但免疫组化证实移植细胞在局部存活了6个月以上。这提示我们,肉眼或常规成像看到的信号减弱,未必代表细胞已死亡,可能仅是标记物表达下调。
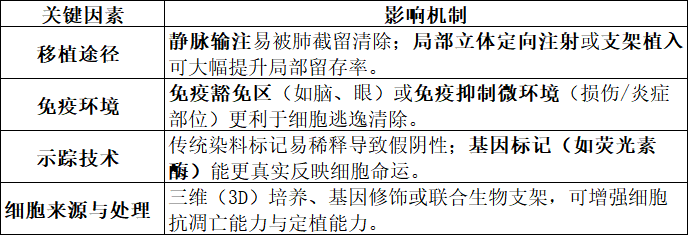
三、为什么有的MSC能“活”得更久?
MSC能否长期存活,并非单一因素决定,而是取决于“细胞+环境+技术”的三角关系:
四、科学启示:从“昙花一现”到“长期驻留”
MSC能存活4个月这一事实,对再生医学具有重要启示:
机制重识:疗效不仅来自短暂的旁分泌,长期存活的细胞可能通过持续分泌营养因子、免疫调节及缓慢分化,实现更持久的修复。
策略优化:对于慢性病(如神经退行性疾病、骨关节炎),通过优化移植技术和联合材料,有望实现“一次治疗,长期受益”,减少重复注射次数。
安全新思:长期存活也意味着需要更严谨的长期安全性随访,评估细胞在体内的终末命运。
结语
MSC绝非只能“昙花一现”。科学正在证明,只要给予合适的“土壤”(微环境)和“播种”方式(移植技术),这些种子细胞完全可以在体内扎根生长,成为长期的“修复工程师”。未来的研究将更加聚焦于如何为MSC创造最佳的长期存活条件,从而最大化其治疗潜力。
免责声明:文章仅用于科普交流,无任何商业目的不作任何商业用途,亦不表示任何医疗声明或建议。我们尊重原创,也注重分享。图文来源网络,版权归原作者所有,如涉及作品内容、版权或其它问题,请联系我们删除!


 闽公网安备 35020602002648 号
闽公网安备 35020602002648 号 QQ 客服
QQ 客服
